Chapter 4. परमाणु की संरचना Class 9 Science CBSE notes in hindi परमाणु मॉडल | जे. जे. टाॅमसन | रदरफोर्ड | नील्स बोर - CBSE Study
कक्षा 9 Science के लिए NCERT समाधान नवीनतम CBSE पाठ्यक्रम और NCERT पाठ्यपुस्तकों के अनुसार सावधानीपूर्वक तैयार किए गए हैं, ताकि विद्यार्थी प्रत्येक अवधारणा को स्पष्ट रूप से समझ सकें। इन समाधानों में सभी महत्वपूर्ण 4. परमाणु की संरचना को विस्तृत व्याख्या और चरण-दर-चरण उत्तरों सहित शामिल किया गया है, जिससे परीक्षा की बेहतर तैयारी हो सके। प्रत्येक परमाणु मॉडल | जे. जे. टाॅमसन | रदरफोर्ड | नील्स बोर को सरल भाषा में समझाया गया है, ताकि विद्यार्थी मूलभूत सिद्धांतों को आसानी से समझकर अपनी शैक्षणिक उपलब्धि में सुधार कर सकें। यह अध्ययन सामग्री दैनिक गृहकार्य, पुनरावृत्ति अभ्यास तथा वार्षिक परीक्षा की तैयारी के लिए विशेष रूप से उपयोगी है। सटीक उत्तर, स्पष्ट अवधारणाएँ और व्यवस्थित सामग्री विद्यार्थियों को आत्मविश्वास बढ़ाने तथा परीक्षाओं में अधिक अंक प्राप्त करने में सहायता करती है। चाहे आप किसी विशेष विषय का पुनरावृत्ति कर रहे हों या पूरे अध्याय की तैयारी कर रहे हों, यह संसाधन Science में पूर्ण सफलता के लिए विश्वसनीय और पाठ्यक्रम-आधारित मार्गदर्शन प्रदान करता है।
CBSE NOTES:
Class 9 English Medium Science All Chapters:
4. परमाणु की संरचना
2. परमाणु मॉडल | जे. जे. टाॅमसन | रदरफोर्ड | नील्स बोर
अध्याय 4. परमाणु की संरचना
टॉमसन का परमाणु मॉडल:
टाॅमसन ने परमाणुओं की संरचना से संबंधित एक माॅडल प्रस्तुत किया, जो क्रिसमस केक की तरह था। इनके अनुसार परमाणु एक धनावेशित गोला था, जिसमें इलेक्ट्राॅन क्रिसमस केक में लगे सूखे मेवों की तरह थे।
तरबूज का उदाहरण भी ले सकते हैं|
जिसके अनुसार परमाणु में धन आवेश तरबूज के खाने वाले लाल भाग की तरह बिखरा है, जबकि इलेक्ट्रॅान धनावेशित गोले में तरबूज के बीज की भांति ध्ँसे हैं |
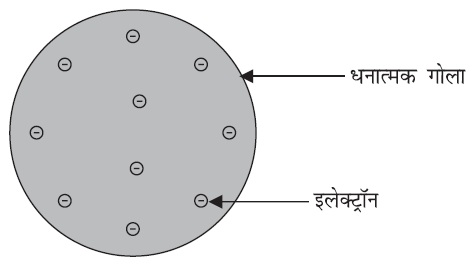
टॉमसन का परमाणु मॉडल
टाॅमसन ने प्रस्तावित किया किः
(i) परमाणु धन आवेशित गोले का बना होता है और इलेक्ट्रॅान उसमें ध्ँसे होते हैं।
(ii) ऋणात्मक और धनात्मक आवेश परिमाण में समान होते हैं। इसलिए परमाणु वैद्युतीय रूप से उदासीन होते हैं।
टॉमसन के परमाणु मॉडल की कमियाँ/सीमाएँ:
(i) दुसरे वैज्ञानिकों द्वारा किये गए प्रयोगों को इस मॉडल के द्वारा नहीं समझाया जा सका |
परमाणु नाभिक की खोज:
परमाणु केन्द्रक की खोज रदरफोर्ड ने की, उन्होने तेज गति से चल रहे अल्फा कणों को सोने की पतली पन्नी पर टकराया गया । जिसके परिणाम से पता चला कि परमाणु में अधिकांश भाग खाली है जहाँ से अल्फा कण बीना टकराये पन्नी से सीधे निकल गये परन्तु कुछ अल्फा कण पन्नी के द्वारा बहुत छोटे कोण से विक्षेपित हुए। जहाँ से ये कण विक्षेपित हुए थे, दरअसल वह परमाणु का नाभिक अर्थात केन्द्रक था । इसप्रकार रदरफोर्ड ने नाभिक की खोज की ।
रदरफोर्ड के परमाणु प्रयोग के परिणाम:
अल्फ़ा कण-प्रकीर्णन प्रयोग ने आशा के बिलकुल विपरीत परिणाम दिया । इससे
निम्नलिखित परिणाम मिले -
(i) तेज गति से चल रहे अधिकतर अल्फ़ा कण सोने की पन्नी से सीधे निकल गए।
(ii) कुछ अल्फ़ा कण पन्नी के द्वारा बहुत छोटे कोण से विक्षेपित हुए।
(iii) आश्चर्यजनक रूप से प्रत्येक 12000 कणों में से एक कण वापस आ गया।
रदरफोर्ड के परमाणु नाभकीय मॉडल के लक्षण:
रदरफोर्ड के प्रयोगो के आधार पर परमाणु का नाभकीय - माॅडल के निम्नलिखित लक्षण थे।
1. परमाणु का केन्द्र धन आवेशीत होता है जिसे नाभिक कहा जाता है।
2. एक परमाणु का लगभग सम्पूर्ण द्रव्यमान नाभिक में होता है।
3. इलेक्ट्रान नाभिक के चारो ओर निश्चित कक्षाओं में चक्कर लगाते है।
4. नाभिक का आकार परमाणु की तुलना में काफी कम होता हैं।
5. परमाणु में इलेक्ट्राॅनो की संख्या प्रोट्राॅनो की संख्या के बराबर होता है।
रदरफोर्ड के परमाणु माॅडल:
रदरफोर्ड ने जो परमाणु माॅडल प्रस्तुत किया उसके अनुसार-
(i) परमाणु के भीतर का अधिकतर भाग खाली है क्योकि अधिकतर अल्फा कण बिना विक्षेपित हुए सोने की पन्नी से बाहर निकल जाते है।
(ii) बहुत कम कण अपने मार्ग से विक्षेपित होते है जिससे यह ज्ञात होता है कि परमाणु में धन आवेशित भाग बहुत कम होता है।
(iii) ये धन आवेशित भाग परमाणु का नाभिक होता है।
(iv) इलेक्ट्राॅन नाभिक के चारों ओर चक्कर लगाते है।
रदरफोर्ड के परमाणु मॉडल की सीमाएँ:
रदरफोर्ड के परमाणु मॉडल के अनुसार;
इलेक्ट्रॉन्स परमाणु के नाभिक के चारों ओर चक्कर लगाते है जैसे- ग्रह सूर्य के चारो ओर चक्कर लगाते है | परन्तु, इलेक्ट्रॉन वृतीय कक्षा में घुमते हुए स्थायी नहीं बने रहेंगे क्योंकि परिक्रमा के दौरान वे त्वरण उत्पन्न करते हैं | इस त्वरण के कारण वे विकिरण के रूप में ऊर्जा मुक्त करेंगे और वे नाभिक की खींचे चले जायेंगे और नाभिक से टकरायेंगे | ऐसी स्थिति में परमाणु अत्यधिक अस्थिर हो जायेगा और नष्ट हो जायेगा | जबकि ऐसी बात नहीं है |
नील्स बोर के परमाणु माॅडल :
नील्स बोर अपने परमाणु माॅडल की निम्न अवधारणाएॅ प्रस्तुत कीं -
(i) इलेक्ट्राॅन केवल कुछ निश्चित कक्षाओं में ही चक्कर लगा सकते है, जिन्हें इलेक्ट्राॅन की विविक्त कक्षा कहते है।
(ii) जब इलेक्ट्राॅन इस विविक्त कक्षा में चक्कर लगाते है तो उनकी उर्जा का विकिरण नहीं होता।

