समस्थानिक :
समस्थानिक किसी तत्व के वे परमाणु होते है जिनकी परमाणु संख्या तो बराबर होती है परन्तु परमाणु द्रव्यमान भिन्न - भिन्न होता है। जैसे- हाइड्रोजन के तीन समस्थानिको के नाम है :
(i) प्रोटियम (H)
(ii) ड्यूट्रीयम (D)
(iii) ट्राईटियम (T)
ये तीन समस्थानिक हाइड्रोजन परमाणु के स्पीशीज हैं |

इसी प्रकार कार्बन के भी तीन समस्थानिक हैं -

क्लोरिन के समस्थानिक:
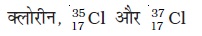
किसी तत्व का प्रत्येक समस्थानिक शुद्ध पदार्थ होता है। समस्थानिकों के रासायनिक गुण समान लेकिन भौतिक गुण अलग-अलग होते हैं।
समस्थानिकों के अनुप्रयोग :
समस्थानिको के उपयोग हम विभिन्न क्षेत्रो में करते है।
1. यूरेनियम के एक समस्थानिक का उपयोग परमाणु भट्टी में ईंधन के रूप में किया जाता है।
2. कैंसर के उपचार में कोबाल्ट के समस्थानिक का उपयोग किया जाता है।
3. घेंघा रोग के इलाज में आयोडिन के समस्थानिक का उपयोग किया जाता हैै।
समभारिक :
ऐसे परमाणु जिनकी द्रव्यमान संख्या समान परन्तु परमाणु संख्या भिन्न - भिन्न होती है।
जैसे - कैल्सियम के परमाणु संख्या 20 तथा आर्गन के परमाणु संख्या18 होती है जबकि दोनो तत्वो के परमाणु द्रव्यमान 40 है। अतः ये दोनों तत्व कैल्सियम तथा ऑर्गन समभारिक है। चूँकि इनका परमाणु संख्या अलग-अलग है परन्तु इनका द्रव्यमान एक सा है |
औसत परमाणु द्रव्यमान : किसी भी तत्व का परमाणु द्रव्यमान वास्तव में उस परमाणु के सभी समस्थानिकों के द्रव्यमान का औसत होता है |
उदाहरण:
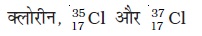
प्रकृति में क्लोरीन दो समस्थानिक रूपों में पाया जाता है, जिसका द्रव्यमान 35u और 37u, जो 3ः 1 के अनुपात में होते हैं।
यहाँ समस्या यह है कि कौन सा परमाणु द्रव्यमान को लिया जाए क्लोरिन 35 या क्लोरिन 37, इसलिए अगर एक तत्व समस्थानिक रूप में उपस्थित होता है तो
हमें प्रत्येक समस्थानिक रूप का प्रतिशत जानना होगा और औसत द्रव्यमान की गणना करनी होगी।
क्लोरीन का औसत परमाणु द्रव्यमान:




